施法迪®抗菌凝胶的作用机理
施法迪®抗菌凝胶的作用机理
关于HPV
HPV是一种细微的DNA病毒,呈球形,无包膜,20面体立体对称结构,表面有72个壳微粒,内含8000个碱基对(bp),分子量为5×106D,其中88%是病毒蛋白,该病毒直径约为45-55nm,它们在机体内都会形成一个难以清除的闭合环状DNA结构(HPV是episome(附加体)形式)。
HPV进入机体后会持续感染以保持基因组完整,随后病毒基因组中的一部分形成episome。之后,病毒就丧失了包装出完整病毒粒子的能力(因为基因组缺失了)。episome会勾在人体基因组中,导致HPV基因组会机会性整合进人体的基因组中。
HPV基因组是双链环状DNA,基因组编码为9个开放读码框架,分为3个功能区:即早期转录区、晚期转录区和非转录区(控制区)。
早期转录区又称为E区,分别编码为E1、E2、E3、E4、E5、E6、E7、E8等8个早期蛋白,具有参与病毒DNA复制、转录、翻译调控和细胞转化等功能。
晚期转录区又称为L区,编码2个衣壳蛋白(即主要衣壳蛋白L1和次要衣壳蛋白L2),组成病毒的衣壳,且与病毒的增殖有关。
非转录区又称为上游调节区、非编码区或长调控区,位于E8和L1之间。该区含有HPV基因组DNA的复制起点和HPV基因表达所必不可少的调控元件,以调控病毒的转录与复制。
HPV基因组的主要功能
|
基因名称 |
主要功能 |
|
E1 |
复制、复制抑制,涉及病毒DNA复制,在病毒开始复制中起关键作用。 |
|
E2 |
激活转录(HPV6、11、16) 抑制转录,结合长控区。是一种反式激活蛋白,涉及病毒DNA转录的反式激活,调节病毒的转录和DNA复制 |
|
E3 |
未知其产物或功能 |
|
E4 |
HPVl引起之疣的细胞蛋白 |
|
E5 |
转化作用(HPV6) |
|
E6 |
协同E7转化作用(HPVl6和HPVl8),主要与病毒细胞转化功能及致癌性有关。 |
|
E7 |
协同E6转化作用(HPVl6和HPVl8) 转录激活(HPVl6),主要与病毒细胞转化功能及致癌性有关。 |
|
E8 |
未知其产物或功能,可能参与复制 |
|
L1 |
主要衣壳蛋白 |
|
L2 |
次要衣壳蛋白 |
|
基因名称 |
主要功能 |
|
E1 |
复制、复制抑制,涉及病毒DNA复制,在病毒开始复制中起关键作用。 |
|
E2 |
激活转录(HPV6、11、16) 抑制转录,结合长控区。是一种反式激活蛋白,涉及病毒DNA转录的反式激活,调节病毒的转录和DNA复制 |
|
E3 |
未知其产物或功能 |
|
E4 |
HPVl引起之疣的细胞蛋白 |
|
E5 |
转化作用(HPV6) |
|
E6 |
协同E7转化作用(HPVl6和HPVl8),主要与病毒细胞转化功能及致癌性有关。 |
|
E7 |
协同E6转化作用(HPVl6和HPVl8) 转录激活(HPVl6),主要与病毒细胞转化功能及致癌性有关。 |
|
E8 |
未知其产物或功能,可能参与复制 |
|
L1 |
主要衣壳蛋白 |
|
L2 |
次要衣壳蛋白 |
|
基因名称 |
主要功能 |
|
E1 |
复制、复制抑制,涉及病毒DNA复制,在病毒开始复制中起关键作用。 |
|
E2 |
激活转录(HPV6、11、16) 抑制转录,结合长控区。是一种反式激活蛋白,涉及病毒DNA转录的反式激活,调节病毒的转录和DNA复制 |
|
E3 |
未知其产物或功能 |
|
E4 |
HPVl引起之疣的细胞蛋白 |
|
E5 |
转化作用(HPV6) |
|
E6 |
协同E7转化作用(HPVl6和HPVl8),主要与病毒细胞转化功能及致癌性有关。 |
|
E7 |
协同E6转化作用(HPVl6和HPVl8) 转录激活(HPVl6),主要与病毒细胞转化功能及致癌性有关。 |
|
E8 |
未知其产物或功能,可能参与复制 |
|
L1 |
主要衣壳蛋白 |
|
L2 |
次要衣壳蛋白 |
关于HPV的DNA(E2、E6、E7)
随着分子生物学的不断进展,近些年来对HPV的各功能区,特别是对E2、E6、E7的研究又有了新的认识。
E6 和 E7 为病毒癌基因,可影响细胞周期的调控,被认为在细胞转化及在肿瘤形成中起着关键作用,参与并调控宿主细胞的病毒基因表达和复制。
E6还能激活端粒酶,使细胞不能正常凋亡。
E6和E7蛋白不仅具有转化和致癌作用,而且还具有对病毒基因和细胞基因转录的反式激活活性。
E6 蛋白与 p53 ,E7 蛋白与 Rb 蛋白结合,使细胞逃脱p53和Rb的控制,导致这两种抑癌基因失活,使通常处于静止状态的细胞增生活跃、肿瘤生长,从而引起正常组织细胞周期发生改变和细胞恶性转化。
现认为E2蛋白是一种特异性的DNA束缚蛋白,可以调节病毒mRNA的转录和DNA的复制,并有减量调节E6、E7表达的作用。
E2蛋白还可以通过结合病毒启动子附近的基因序列而抑制转录起始。
当E2完整性遭到破坏后,负反馈调节功能也即消失,引起致癌性基因E6、E7过量表达,从而导致癌变的顺向推进。
在HPV整合过程中,许多基因被破坏或缺失,其中E2基因受到的破坏最为严重。E2基因破坏是由 HPV整合引起导致宫颈病变进行性进展的一个重要事件,并且E2基因的破坏程度与宫颈病变的进展呈正相关性。
总之,在HPV诱导的肿瘤中,HPV病毒基因随机整合到宿主染色体内,导致E2基因破坏和E2基因低水平表达或表达缺失,造成HPV病毒生命周期的中止,及对致癌基因 E6和 E7调节的紊乱,E2缺失解除了对E6、E7表达的抑制,这是肿瘤基因起源的关键一步。因此,作为保护性蛋白 E2基因一旦被破坏,势必造成宫颈病变的恶性进程。
由上可知,在HPV病毒中,E6、E7、E2蛋白在病毒复制和致癌机制中起到至关重要的作用。那么,控制E2蛋白可以作为我们研究杀灭病毒的突破口。
施法迪®抗菌凝胶作用
盛华医药在2005年的专利中就已经对染色体病毒的感染、传播、复制机制进行详尽研究和阐述,提出通过控制整合酶和病毒蛋白的方法清除HPV以及HIV病毒的理论思路,该研究获得全球在内包括中国88个国家的专利,并根据专利的理论研制出施法迪®抗菌凝胶产品。
在作用机理上充分体现专利研究中对病毒控制的思路和方法,通过增强E2蛋白而达到抑制E6、E7蛋白的目标,使E6无法实现阻止病毒凋亡等功能、E7无法实现让细胞永生化等功能,从而实现让病毒无法复制并引导病毒凋亡。施法迪产品在临床上也进行了充分验证,对HPV病毒呈现高效的杀灭作用。
施法迪®抗菌凝胶机理
2015年,盛华医药委托CRO进行了施法迪产品对基因影响的深入研究实验。
通过产品, 深入验证HPV病毒中各蛋白的功能和机理,杀灭HPV病毒以及对人类子宫颈癌的作用机理和效果,并对宫颈癌CIN1和CIN2阶段的药理机制进行研究。
我们用real-time PCR 方法,检测施法迪产品和阳性对照物Aphidicolin处理过的CaSki细胞和SiHa细胞(均为人子宫颈癌细胞)中HPV16 E6,HPV16 E7以及CaSki细胞中HPV16 E2的基因量和mRNA量。
从下图实验数据显示,施法迪产品对HPV E2蛋白不仅没有抑制作用,在48小时的实验数据中,更显示对E2有明显的增强作用。
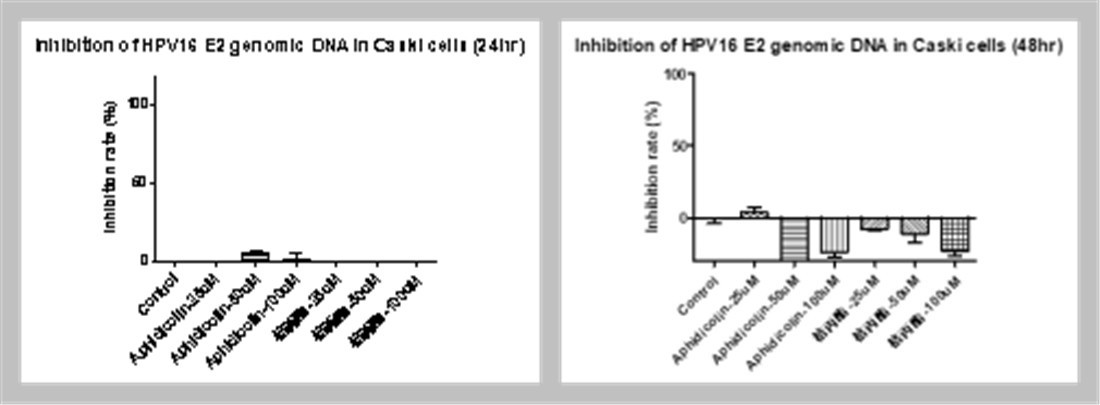
从下图实验数据还看出,施法迪产品对HPV E6蛋白的抑制率达到90.89,对E7蛋白的抑制率达到94.51。由此可见产品对E6蛋白和E7蛋白均有强力的抑制作用。(X轴是剂量,Y轴是抑制率)

由上述实验数据可清晰看出,经施法迪产品处理的Caski细胞和SiHa细胞(均为人子宫颈癌细胞),在48小时能显著抑制细胞中HPV16 E6 和 HPV16 E7 基因量和mRNA量。
且处理48小时后,HPV16 E2 基因量升高,从而能显著抑制CaSki细胞和SiHa细胞中HPV16 E6和 HPV16 E7基因量和mRNA量。
同时,我们用real-time PCR 方法检测施法迪处理过的Hela细胞中HPV18 L1的基因量和mRNA量。 研究表明,施法迪能显著抑制Hela细胞中HPV18 L1 基因量和mRNA量。
最后,我们测试了C33-A细胞(人子宫颈癌细胞)中HPV16 E2, HPV16 E6, HPV16 E7 及HPV18 L1的基因量和mRNA量,表明C33-A细胞(人子宫颈癌细胞)为HPV阴性细胞(实验结束)。
经过上述实验,充分证明施法迪®产品对HPV病毒以及人子宫颈癌中的HPV病毒有显著的抑制和杀灭作用。





